A fotobiomodulação transcraniana (FBMt ou tPBM) vem ganhando espaço na prática clínica e na pesquisa acadêmica por oferecer uma forma não invasiva de estimular o tecido cerebral com luz em comprimentos de onda específicos. Mas, uma pergunta continua central: por que a literatura científica insiste tanto no uso da luz infravermelha próxima?
A resposta não está em preferência de mercado, estética do dispositivo ou tendência tecnológica. Ela está na física dos tecidos biológicos e na biologia celular. Em outras palavras: a escolha do infravermelho próximo é técnica, não arbitrária.
Hoje, a fotobiomodulação cerebral é estudada com luz entre o vermelho e o infravermelho, em geral dentro da faixa de 600 a 1100 nm. Ainda assim, quando se fala em aplicação transcraniana, os comprimentos de onda no infravermelho próximo, especialmente em torno de 810 nm, aparecem de forma recorrente porque equilibram dois fatores decisivos: capacidade de penetração nos tecidos e interação biológica relevante com alvos mitocondriais.,

O que é a fotobiomodulação transcraniana?
A fotobiomodulação transcraniana consiste na aplicação de luz de baixa intensidade sobre o couro cabeludo com o objetivo de entregar fótons ao sistema nervoso central. A proposta é que parte dessa energia luminosa atravesse as camadas extracerebrais e alcance regiões corticais, desencadeando respostas bioquímicas e metabólicas associadas à função neuronal.
Entre os mecanismos mais discutidos está a interação da luz com a citocromo c oxidase, complexo IV da cadeia respiratória mitocondrial. Essa interação está associada:
- ao aumento da atividade mitocondrial;
- à melhora da produção de ATP;
- à modulação do estado redox;
- e a efeitos secundários sobre fluxo sanguíneo, neuroinflamação e sinalização celular.
Também em publicações recentes, a fotobiomodulação transcraniana segue sendo descrita como uma modalidade de neuromodulação com efeitos sobre neurônios, vasos e acoplamento neurovascular.
Porém, para que isso ocorra de forma clinicamente plausível, não basta haver um alvo biológico sensível à luz. A luz precisa chegar até ele.
Os dispositivos de FBMt mais recomendados pelos profissionais de saúde. Confira aqui.
A grande questão: a luz consegue atravessar o crânio?
Essa é a pergunta que define toda a lógica dos parâmetros em FBMt.
Entre a fonte luminosa e o córtex existem várias barreiras: couro cabeludo, sangue, osso craniano, líquor e outras estruturas extracerebrais. Cada uma delas absorve, reflete e dispersa parte da energia incidente. Por isso, a luz que chega ao cérebro é sempre uma fração da luz emitida na superfície.
A literatura experimental e de modelagem mostra que a transmissão transcraniana existe, mas é fortemente dependente do comprimento de onda. Estudos em modelo cadavérico demonstraram que a luz no infravermelho próximo penetra tecidos moles, osso e parênquima cerebral de forma mensurável, enquanto a transmissão da luz vermelha foi muito menor nas mesmas condições.
Em estudo comparativo com crânios humanos e de outras espécies, a transmissão de 800 nm caiu conforme a espessura óssea aumentou, reforçando que a barreira craniana não é “opaca”, mas altamente atenuante e anatomicamente variável.
Ou seja: a luz pode atravessar o crânio, mas isso depende de usar uma faixa espectral que atravesse os tecidos com menor perda relativa.
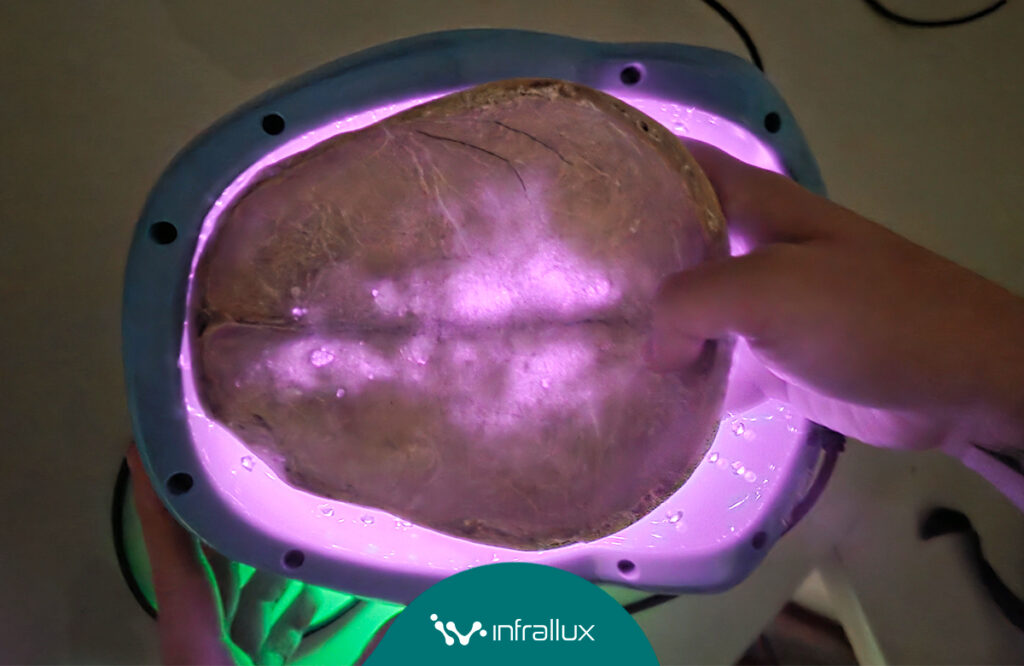
Foto: Equipe Infrallux (2026)
A janela óptica terapêutica dos tecidos biológicos
É aqui que entra um conceito central para qualquer profissional de saúde que queira entender FBMt em profundidade: a chamada janela óptica terapêutica, também conhecida como janela óptica dos tecidos biológicos.
Em determinadas faixas do espectro, a luz é menos absorvida pelos principais cromóforos teciduais, especialmente hemoglobina, melanina e água. Quando a absorção por esses componentes cai, a luz tende a atravessar o tecido com maior profundidade relativa. É justamente nessa “janela” que a fotobiomodulação transcraniana opera com mais racionalidade física.
Na prática, isso significa o seguinte:
- No vermelho mais baixo, a absorção por hemoglobina ainda é mais relevante, o que limita a propagação em profundidade.
- Já em comprimentos de onda mais altos, sobretudo acima de aproximadamente 950 nm, a absorção pela água aumenta de forma importante.

Vermelho ou infravermelho próximo: qual a diferença na prática?
Tanto a luz vermelha quanto a infravermelha podem ser usadas em fotobiomodulação. O problema é que “poder ser usada” não significa “ser a melhor escolha para atravessar o crânio”.
Para aplicações mais superficiais, como pele, mucosa, cicatrização e estruturas menos profundas, a luz vermelha pode desempenhar papel relevante. Já para o cérebro, a situação muda. A meta não é apenas interagir com tecido biológico; é alcançar o tecido cerebral após atravessar barreiras anatômicas densas.
Nesse contexto, estudos de transmissão comparando 633 nm e 830 nm mostraram vantagem clara do infravermelho próximo.
- Em seções coronais de crânio cadavérico, a porcentagem de penetração foi maior em 830 nm do que em 633 nm;
- O mesmo padrão apareceu em seções sagitais com tecido mole intacto, nas quais a luz infravermelha atravessou de forma mensurável, enquanto a luz vermelha foi mínima ou quase desprezível em alguns pontos.
Isso ajuda a entender por que, na prática clínica e nos dispositivos para cérebro, a luz vermelha costuma aparecer menos como protagonista do componente transcraniano principal e mais como complemento de protocolos ou de sistemas mistos.
E o comprimento de onda de 1064 nm? Penetra mais?
Essa é uma discussão importante.
Há estudos e linhas de pesquisa que utilizam 1064 nm, especialmente em protocolos de neuromodulação e cognição. A justificativa mais comum é a menor dispersão óptica em comprimentos de onda mais altos. Isso faz sentido físico e ajuda a explicar por que 1064 nm segue sendo uma faixa relevante na pesquisa contemporânea. Inclusive, trabalhos e revisões recentes continuam explorando FBMt com 1064 nm em humanos.
Por outro lado, a grande vantagem do comprimento de 810 nm e semelhantes não é superar o 1064 nm em deposição média de luz nos alvos corticais, mas sim a sua superioridade biológica: essa faixa coincide com os picos de absorção do cromóforo citocromo c oxidase (CCO), atuando de forma mais direta e otimizada no metabolismo mitocondrial.
O papel da anatomia: nem todo crânio transmite igual
Outro ponto essencial para profissionais de saúde: a transmissão transcraniana não depende apenas do aparelho. Depende também do paciente.
Espessura do couro cabeludo, densidade e espessura do osso, distância até o córtex, presença de seios paranasais e características regionais da cabeça influenciam a dosimetria.
Simulações baseadas em atlas de diferentes idades (um molde digital que representa como essa anatomia costuma ser naquela faixa etária) mostraram redução progressiva da deposição de energia com o envelhecimento, sobretudo por aumento da espessura extracerebral2.
Isso muda a forma de pensar a FBMt. Não basta perguntar “qual é o comprimento de onda?”. Também é preciso perguntar “em quem?”, “em que região?”, “com qual densidade de potência?” e “com qual desenho de emissão?”.
Por que o LED faz sentido na aplicação clínica?
Ao falar de penetração, muita gente pensa imediatamente em laser. Todavia, dispositivos com LEDs têm vantagens concretas na FBMt, especialmente quando o objetivo é cobrir áreas maiores do couro cabeludo de forma prática, segura e escalável em consultório.
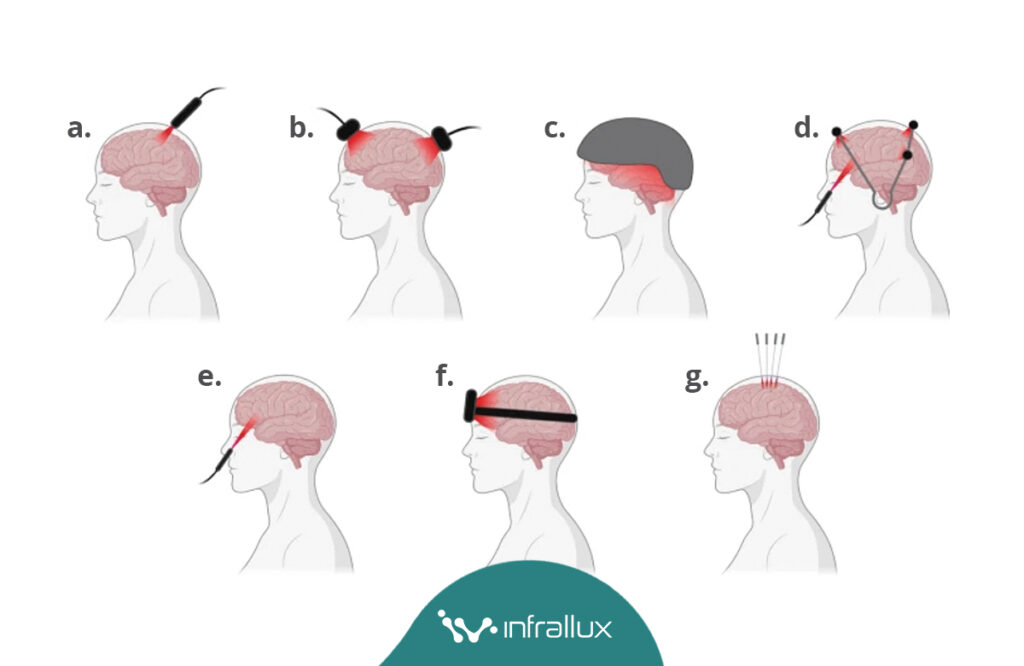
Fonte: ERNANDES, F.; OLIVEIRA, S.; MONTEIRO, F. et al. Devices used for photobiomodulation of the brain—a comprehensive and systematic review. Journal of NeuroEngineering and Rehabilitation, [S.l.], v. 21, p. 53, 2024. Disponível em: https://jneuroengrehab.biomedcentral.com/articles/10.1186/s12984-024-01351-8. Acesso em: 20 mar. 2026.
A revisão sistemática de dispositivos para FBM cerebral mostra grande diversidade de arquiteturas, incluindo clusters, capacetes e sistemas localizados com LEDs. Entre as vantagens mais citadas estão ampla área de atuação, possibilidade de uso domiciliar, facilidade de posicionamento e estímulo simultâneo de múltiplas regiões.
Na prática clínica, isso é relevante porque o LED permite dispositivos “vestíveis” (wearables), de uso mais confortável e com melhor adaptabilidade a protocolos repetidos. Para aplicações transcranianas, em que a regularidade do tratamento e a cobertura anatômica importam, esse formato faz bastante sentido.
Conheça os dispositivos pioneiros em FBMt no Brasil. Clique aqui.
O que os estudos mais recentes sobre FBMt reforçam?
As publicações mais recentes não mudaram o fundamento físico da fotobiomodulação transcraniana; elas o reforçaram.
Em 2025 e 2026, a literatura segue descrevendo a FBMt como uma estratégia de neuromodulação baseada sobretudo em luz vermelha e infravermelha próxima, com foco em metabolismo celular, citocromo c oxidase, hemodinâmica e acoplamento neurovascular.
Revisões recentes destacam justamente esses mecanismos e o papel da FBMt na modulação da função cerebral,.
Estudos experimentais recentes também continuam usando 810 nm e 1064 nm, o que mostra que o debate atual não é se a luz deve estar no vermelho/infravermelho, mas como otimizar dose, alvo e geometria óptica.
Conclusão
A luz infravermelha próxima é amplamente utilizada na fotobiomodulação transcraniana porque oferece uma combinação especialmente valiosa para o cérebro: consegue atravessar com mais eficiência relativa os tecidos biológicos do que a luz vermelha visível em aplicações transcranianas e, ao mesmo tempo, mantém relevância biológica para mecanismos mitocondriais associados à FBMt.
Em outras palavras, o infravermelho próximo não é usado “porque funciona melhor” de forma vaga. Ele é usado porque a física da propagação da luz nos tecidos e a biologia da resposta celular apontam nessa direção.
Para o profissional de saúde, esse entendimento é importante, porque ajuda a separar a FBMt séria da FBMt genérica, sem os parâmetros ideais. Em cérebro, comprimento de onda importa. Janela óptica importa. Anatomia importa. E dispositivo também importa.
Quando esses elementos são respeitados, a escolha do infravermelho próximo deixa de parecer uma decisão comercial e passa a ser reconhecida pelo que realmente é: uma decisão fundamentada em evidência física e biológica.

Referências bibliográficas
- FERNANDES, Filipa et al. Devices used for photobiomodulation of the brain — a comprehensive and systematic review. Journal of NeuroEngineering and Rehabilitation, v. 21, n. 53, 2024. Disponível em: https://doi.org/10.1186/s12984-024-01351-8. Acesso em: 13 abr. 2026.
- YUAN, Yaoshen et al. Transcranial photobiomodulation with near-infrared light from childhood to elderliness: simulation of dosimetry. Photobiomodulation, Photomedicine, and Laser Surgery, 2020. Disponível em: https://pmc.ncbi.nlm.nih.gov/articles/PMC7039173/. Acesso em: 13 abr. 2026.
- YAN, Bingzi et al. Unlocking the potential of photobiomodulation therapy for brain neurovascular coupling: the biological effects and medical applications. Journal of Cerebral Blood Flow & Metabolism, v. 45, n. 5, p. 800–830, 7 jan. 2025. Disponível em: https://pmc.ncbi.nlm.nih.gov/articles/PMC11705326/. Acesso em: 13 abr. 2026.
- JAGDEO, Jared R. et al. Transcranial red and near infrared light transmission in a cadaveric model. PLoS ONE, 2012. Disponível em: https://pmc.ncbi.nlm.nih.gov/articles/PMC3471828/. Acesso em: 13 abr. 2026.
- LAPCHAK, Paul A. et al. Transcranial near-infrared laser transmission (NILT) profiles (800 nm): systematic comparison in four common research species. PLoS ONE, 2015. Disponível em: https://pubmed.ncbi.nlm.nih.gov/26039354/. Acesso em: 13 abr. 2026.
- YUE, Lan; HUMAYUN, Mark S. Monte Carlo analysis of the enhanced transcranial penetration using distributed near-infrared emitter array. Journal of Biomedical Optics, v. 20, n. 8, p. 088001, 2015. Disponível em: https://www.spiedigitallibrary.org/journals/journal-of-biomedical-optics/volume-20/issue-08/088001/Monte-Carlo-analysis-of-the-enhanced-transcranial-penetration-using-distributed/10.1117/1.JBO.20.8.088001.full. Acesso em: 13 abr. 2026.
- BASTOLA, Subrat et al. Transcranial 1064-nm laser photobiomodulation modulates frequency-specific cortical source dynamics and functional connectivity in healthy adults. Frontiers in Human Neuroscience, v. 19, 7 jan. 2026. Disponível em: https://doi.org/10.3389/fnhum.2025.1704482. Acesso em: 13 abr. 2026.
- YAN, Bingzi et al. Unlocking the potential of photobiomodulation therapy for brain neurovascular coupling: the biological effects and medical applications. Journal of Cerebral Blood Flow & Metabolism, v. 45, n. 5, p. 800–830, maio 2025. Publicado online em 7 jan. 2025. Disponível em: https://pubmed.ncbi.nlm.nih.gov/39763390/. Acesso em: 13 abr. 2026.
- TANG, Lifeng et al. Application of non-invasive transcranial photobiomodulation in ischemic stroke: mechanisms and current insights. iScience, v. 29, n. 1, p. 114254, 16 jan. 2026. Disponível em: https://www.sciencedirect.com/science/article/pii/S2589004225025155. Acesso em: 13 abr. 2026.


