Durante décadas, transtornos como o Transtorno do Espectro Autista (TEA), o TDAH e o Transtorno Opositivo Desafiador (TOD) foram lidos exclusivamente pela lente do comportamento. Hoje, revisões sistemáticas mostram que essas condições compartilham um substrato biológico comum: disfunção mitocondrial, aumento do estresse oxidativo e neuroinflamação crônica de baixo grau. Nesse contexto, fotobiomodulação transcraniana e transtornos do neurodesenvolvimento deixam de ser temas desconectados: a fotobiomodulação transcraniana (FBMt) passa a se apresentar como uma intervenção com plausibilidade biológica para modular justamente as vias metabólicas e inflamatórias implicadas nesses quadros.
As mitocôndrias, responsáveis pela produção de ATP, apresentam atividade reduzida dos complexos da cadeia de transporte de elétrons em crianças com TEA1. Quando a função mitocondrial falha, o impacto ocorre através de diversas alterações sistêmicas, neurológicas e metabólicas. O resultado clínico? Dificuldade de atenção, atrasos no processamento da fala e comportamentos repetitivos.
Paralelamente, a microglia (célula imune residente do cérebro) entra em ativação crônica, liberando citocinas pró-inflamatórias (como TNF-α, IL-6 e IL-1β) que contribuem para a perda de conexões sinápticas2. Estudos de neuroimagem confirmam o que se descreve como subconectividade no autismo: uma diminuição na conectividade funcional, caracterizada principalmente por falhas nas conexões de longo alcance entre diferentes regiões cerebrais.
Esse é o terreno biológico. E é exatamente aqui que a fotobiomodulação transcraniana entra.
Fotobiomodulação transcraniana e transtornos do neurodesenvolvimento: como a luz age no cérebro? O mecanismo central
A fotobiomodulação (PBM), que possui diversas aplicações, incluindo a via transcraniana, utiliza luz em comprimentos de onda vermelho e infravermelho próximo (NIR) para estimular processos celulares. O mecanismo primário, descrito por Hamblin (2017), envolve a absorção de luz pelo citocromo c oxidase (CCO), localizado na mitocôndria3; confirmado por múltiplas revisões, envolve o citocromo c oxidase (CCO), um complexo proteico da cadeia respiratória mitocondrial.
Essas alterações metabólicas e o aumento energético disparam cascatas de sinalização celular que incluem a ativação de diversos fatores de transcrição (como o NF-kB e o HIF-1a), resultando em respostas celulares de longa duração que promovem a sobrevivência, a proteção e a reparação dos tecidos.4
Na aplicação transcraniana (FBMt), a luz atravessa estruturas como o couro cabeludo e o crânio para atingir a superfície cortical. A terapia atua em uma janela óptica em que há menor absorção por melanina e água, sendo o comprimento de 810 nm frequentemente apontado como o de penetração mais profunda e maior absorção pelo alvo celular.
Em indivíduos mais jovens (como em recém-nascidos), a penetração da luz no tecido cerebral chega a ser de duas a três vezes maior, fator que está fortemente associado ao menor grau de mielinização do cérebro nessa fase, contrastando com a perda de penetração vista no envelhecimento devido ao aumento da espessura dos tecidos.5,6
Os comprimentos de onda nas regiões do vermelho e do infravermelho próximo (NIR, 750–850 nm) correspondem aos picos de absorção do citocromo c oxidase (CCO). Comprimentos específicos na faixa NIR, como o de 810 nm, atuam predominantemente via CCO para estimular a proliferação celular, diferenciando-se de comprimentos maiores (como 980 nm), que atuam através do aquecimento da água intracelular e da ativação de canais iônicos sensíveis ao calor.7
Fotobiomodulação transcraniana e transtornos do neurodesenvolvimento: o que os estudos clínicos mostram até agora
TEA: resultados preliminares promissores em crianças e adultos
Há estudos-piloto e retrospectivos; seus achados são encorajadores o suficiente para justificar investigações mais robustas.
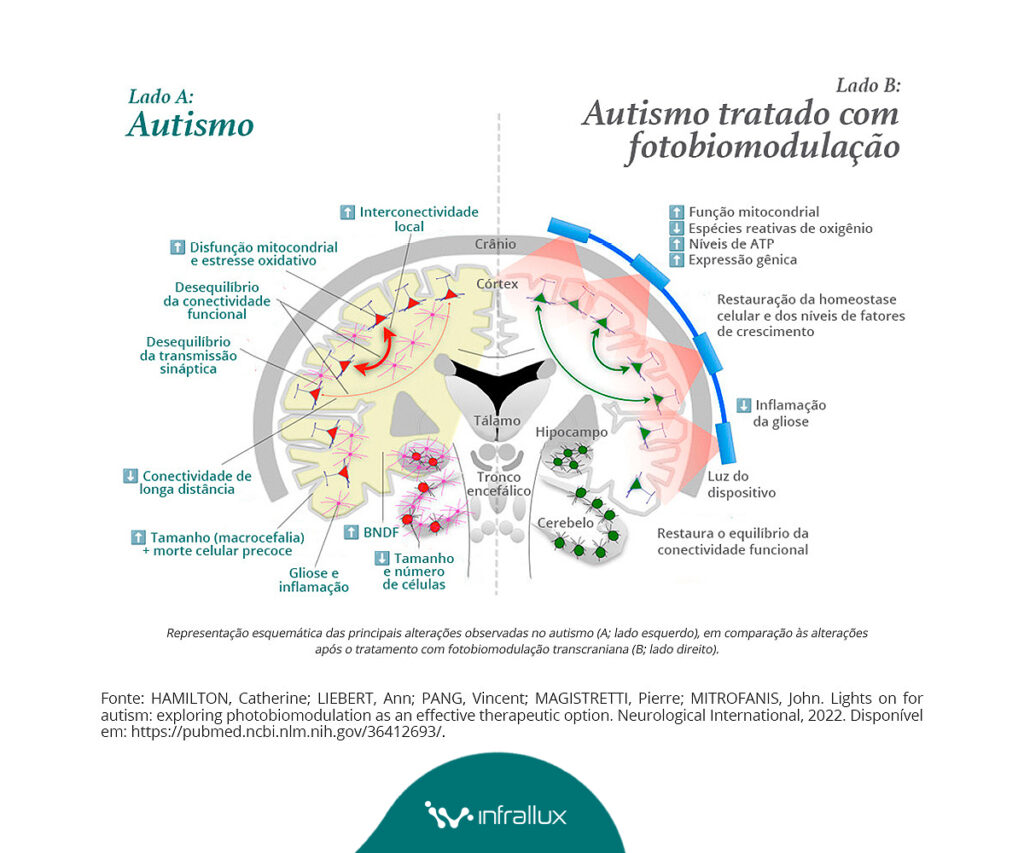
Representação esquemática das principais alterações neurobiológicas descritas no autismo (lado A), como disfunção mitocondrial, estresse oxidativo, neuroinflamação e desequilíbrios de conectividade, e dos alvos terapêuticos propostos para a fotobiomodulação transcraniana (lado B), com foco em restauração da bioenergética, modulação inflamatória e reorganização funcional de redes cerebrais.
Em crianças, um estudo retrospectivo com 21 pacientes com TEA tratados com fotobiomodulação transcraniana relatou redução significativa da gravidade dos sintomas na CARS, com melhora de sono, atenção, rigidez comportamental e estresse parental medido pelo APSI e outros instrumentos.8
Em adultos com TEA de alto funcionamento, um estudo aberto de 8 semanas com 10 participantes mostrou queda significativa nos escores totais do SRS‑2, e 50% atingiram critério de resposta clínica ao final do protocolo.9
De forma consistente entre esses trabalhos, os relatos clínicos incluem maior engajamento social, redução de irritabilidade e comportamentos desafiadores, melhora da comunicação e da atenção, além de padrão de sono mais estável em parte das crianças.
TDAH: uma linha de pesquisa em construção
No TDAH, a fotobiomodulação transcraniana ainda está em fase exploratória, mas os resultados apontam melhora de atenção, controle inibitório e regulação emocional em parte dos pacientes.
Uma série de casos com aplicação de laser vermelho e luz infravermelha próxima em região frontal descreveu redução de sintomas de desatenção e hiperatividade já nas primeiras sessões, sem eventos adversos relevantes. Os autores sugerem que a melhora na função mitocondrial e o aumento do fluxo sanguíneo podem ter impacto funcional na conectividade cerebral associada ao TDAH, particularmente na rede de modo padrão (default mode network) e nas redes frontais.10
TOD: uma hipótese teórica
No Transtorno Opositivo Desafiador (TOD), ainda não existem estudos clínicos desenhados especificamente para avaliar fotobiomodulação transcraniana como tratamento primário, mas alguns trabalhos em TEA e TDAH sugerem uma melhora indireta de comportamentos opositores, irritabilidade e agressividade dentro de quadros de neurodesenvolvimento mais amplos.
Em crianças com TEA e comorbidades comportamentais (irritabilidade, agressividade, traços opositores), os estudos de FBMt já citados neste artigo relatam melhora de comportamento disruptivo e de manejo familiar, sugerindo impacto indireto sobre sintomas tipo TOD.
Há também um estudo de caso de FBMt em um jovem adulto (24 anos) com mutação no gene SCN2A que descreve, entre outros aspectos, traços opositores e impulsividade, com relato de melhora comportamental global (redução de impulsividade e rigidez) após o protocolo.11
Fotobiomodulação transcraniana e transtornos do neurodesenvolvimento: o ILIB Sublingual pode ser usado nesses casos?
Até o momento, não existem estudos clínicos específicos avaliando ILIB sublingual em crianças com TEA, TDAH ou TOD, mas há evidências de que a irradiação sistêmica do sangue (ILIB ou técnicas equivalentes, como intranasal) modula justamente vias envolvidas nesses quadros: função mitocondrial, reologia sanguínea, inflamação e perfusão cerebral.12
A terapia ILIB entra como uma estratégia adjuvante aplicada de forma não invasiva na artéria radial. Estudos mostram que a técnica melhora a oxigenação sistêmica do sangue e promove a síntese de ATP (energia celular), atuando diretamente no fortalecimento do sistema imunológico e no controle do processo inflamatório
Quando colocamos esses achados ao lado das evidências de que a FBMt melhora sintomas e marcadores eletrofisiológicos em TEA e TDAH, a hipótese clínica passa a ser coerente: usar a FBMt para modular diretamente circuitos corticais e o ILIB sublingual para otimizar, em paralelo, o ambiente sistêmico (perfusão, resposta imune, bioenergética) que sustenta esse cérebro vulnerável, sempre como terapia coadjuvante e não substitutiva às intervenções comportamentais e farmacológicas estabelecidas.
Alto perfil de segurança da FBMt
O perfil de segurança da FBMt é um de seus pontos fortes. Não há registro de eventos adversos graves em estudos pediátricos. Porém, efeitos leves são documentados — hiperatividade transitória, cefaleia e insônia em alguns participantes.
As contraindicações reconhecidas incluem fotossensibilidade extrema e aplicação sobre neoplasias ativas. Diferentemente de correntes elétricas, a luz não provoca dor nem desconforto significativo, o que favorece a adesão na população pediátrica.
Este conteúdo tem caráter informativo e educacional. Não substitui avaliação, diagnóstico ou tratamento médico. Consulte sempre um profissional de saúde habilitado.
Referências consultadas
1- FRYE, Richard E. et al. Biomarkers of mitochondrial dysfunction in autism spectrum disorder: a systematic review and meta-analysis. Neurobiology of Disease, Amsterdã, v. 197, p. 106520, jul. 2024. Disponível em: <https://www.sciencedirect.com/science/article/pii/S0969996124001190>. Acesso em: 16 mar. 2026.
2- RODRIGUEZ, Juan I.; KERN, Janet K. Evidence of microglial activation in autism and its possible role in brain underconnectivity. Neuron Glia Biology, Cambridge, v. 7, n. 2–4, p. 205–213, maio 2011. Disponível em: <https://pmc.ncbi.nlm.nih.gov/articles/PMC3523548/>. Acesso em: 16 mar. 2026.
3- HAMBLIN, Michael R. Mechanisms and applications of the anti-inflammatory effects of photobiomodulation. AIMS Biophysics, Springfield, v. 4, n. 3, p. 337–361, 19 maio 2017. Disponível em: <https://www.aimspress.com/article/10.3934/biophy.2017.3.337>. Acesso em: 16 mar. 2026.
4- HAMBLIN, Michael R. Mechanisms and mitochondrial redox signaling in photobiomodulation. Photochemistry and Photobiology, Hoboken, v. 93, n. 6, p. 1263–1270, 22 nov. 2017. Disponível em: <https://onlinelibrary.wiley.com/doi/10.1111/php.12864>. Acesso em: 16 mar. 2026.
5- SALEHPOUR, Farzad et al. Brain photobiomodulation therapy: a narrative review. Molecular Neurobiology, Nova Iorque, v. 55, n. 8, p. 6601–6636, 11 jan. 2018. Disponível em: <https://pmc.ncbi.nlm.nih.gov/articles/PMC6041198/>. Acesso em: 16 mar. 2026.
6- SALEHPOUR, Farzad et al. Penetration profiles of visible and near-infrared lasers and light-emitting diode light through the head tissues in animal and human species: a review of literature. Photobiomodulation, Photomedicine, and Laser Surgery, New Rochelle, v. 37, n. 10, p. 623–636, 23 out. 2019. Disponível em: <https://journals.sagepub.com/doi/10.1089/photob.2019.4676>. Acesso em: 16 mar. 2026.
7- HAMBLIN, Michael R.; LIEBERT, Ann. Photobiomodulation therapy mechanisms beyond cytochrome c oxidase. Photobiomodulation, Photomedicine, and Laser Surgery, New Rochelle, v. 40, n. 2, p. 75–77, 16 fev. 2022. Disponível em: <https://journals.sagepub.com/doi/full/10.1089/photob.2021.0119>. Acesso em: 16 mar. 2026.
8- PALLANTI, Stefano et al. Transcranial photobiomodulation for the treatment of children with autism spectrum disorder (ASD): a retrospective study. Children (Basel), Basel, v. 9, n. 5, p. 755, 20 maio 2022. Disponível em: <https://pmc.ncbi.nlm.nih.gov/articles/PMC9139753/>. Acesso em: 16 mar. 2026.
9- CERANOGLU, Tolga Atilla et al. Transcranial photobiomodulation in adults with high-functioning autism spectrum disorder: positive findings from a proof-of-concept study. Photobiomodulation, Photomedicine, and Laser Surgery, New Rochelle, v. 40, n. 1, p. 4–12, jan. 2022. Disponível em: <https://pubmed.ncbi.nlm.nih.gov/34941429/>. Acesso em: 16 mar. 2026.
10- STEPHAN, William et al. Efficacy of photobiomodulation for attention deficit hyperactivity disorder (ADHD): case studies. World Journal of Neuroscience, Irvine, v. 12, n. 3, p. 215–229, ago. 2022. Disponível em: <https://www.scirp.org/journal/paperinformation?paperid=119187>. Acesso em: 16 mar. 2026.
11- PALLANTI, Stefano; MURETTI, Alessandra. Transcranial photobiomodulation in a single case of gene SCN2A-related autism. Annals of Scientific Reports, Florença, v. 1, 2022. Disponível em: <https://annscri.org/articles/SCR-1027.html>. Acesso em: 16 mar. 2026.
12- SILVA, Vanessa Guerling da; MARTINS, Wesley. The systemic action of the intravascular laser irradiation of blood (ILIB) therapy to strengthen the immune system and the inflammatory process: an integrative review. Research, Society and Development, Itajaí, v. 12, n. 6, e42265, jun. 2022. Disponível em: <https://rsdjournal.org/rsd/article/view/42265>. Acesso em: 16 mar. 2026.



